|
CİLT YAŞLANMASI
Yazar : Mina YAAR*
Çeviren : Öğr. Gör. Hasret ALTINTAŞ**
Yaşlanma; hücrenin zayıflaması, hücre rezervlerinin azalması ve normal hücre fonksiyonlarının oluşumunda aksamayla seyreden karmaşık bir süreçtir. Bu zayıflamalar organizmayı hastalıklara daha yatkın kılar ve yaşamla uyumsuzlaştırır. Canlı türlerinde yaşlanma hızı kabaca standarttır. Öyle ki, yaşlanma bir çeşit önceden tasarlanmış bir olgudur (genetik bir programın neticesi gibi ya da türlerin genetik özelliklerine göre planlanmış bir saat gibi) (1).
Başka bir deyimle, yaşlanma; genetik yatkınlığın yanısıra, fonksiyonlarda azalma, homeostatik bozukluklar ve ölümle sonuçlanan gen ve proteinlerdeki kumulatif harabiyet olarak da tanımlanabilir.
YAŞLANMA - GENETİK PROGRAM
DNA'nın yapısında bir hücrenin yaşlanmadan önce kaç kere bölünebileceğini daha önce belirleyebilen genetik bir sistem vardır. Hücre bölünme sayısını sınırlandıran yapılara telomer (2) denir.
Telomerler, birçok karşılıklı kısa sıra tekrarlarından oluşan eukoryotic kromozomların bağlantı kısımlarıdır (TTAGGG). Hücreler mitoz bölünmeleri sırasında; DNA polimeraz enzimi her bir kromozomun son kısım çiftlerini kopyalayamazlar ve bu da her hücre bölünmesinden sonra kromozomun son kısmının kısalmasıyla sonuçlanır.
Sonuç olarak, kısa olan telomerler gen transkripsiyonlarını pasifleştirir ve hücresel yaşlılığın ya da Apopitozisin (3, 4) işaretlerini verir. Böylece telomer kısalması hücrenin fonksiyonel yaşamını daha önceden belirleyen "iç saat" olarak kabul edilebilir.
YAŞLANMA OLGUSU
İç ve dış faktörlerden kaynaklanan DNA harabiyetinin yaşlanma sürecinde önemli bir rol oynadığı görülmektedir. DNA'nın yıpranması ile ilgili ipuçları Werner, Cockayne ve ataxia telangiectasia (5) gibi erken yaşlanma hastalıklarından elde edilen bulgularla çözümlenmiştir. Bu sendromlardan etkilenen genler DNA harabiyetinin onarılması veya tanınmasına katılan proteinleri kodlarlar (6, 8). Ayrıca az gelişmiş organizmalarda yaşamı belirleyen genler UV (9) ve oksidatif stress (10) gibi DNA harabiyetine yol açan çevresel ajanlara karşı büyük direnç gösteren proteinleri kodlarlar. DNA harabiyeti ve harabiyeti onarma yeteneğinde azalma yaşlanma
olayına neden olur.
Endojen yıpranma işlemine en fazla katkı yapan unsur oksidatif DNA harabiyetidir yani aerobik hücresel metabolizmanın sürekli olarak ürettiği reaktif oksijen türevleri (ROS) neticesidir (1). Hücresel antioksidan defans sistemlerine rağmen ROS'lar sürekli olarak hücresel elemanları tahrip ederler ve zamanla DNA ve diğer biyolojik moleküllerde kümülatif harabiyete neden olurlar. Endojen DNA harabiyetinin yanı sıra cilt, çevresel unsurlarla sürekli temasta olduğundan özellikle ekzojen tahrip edici ajanlara da maruz kalır.
Örneğin hücresel DNA tarafından emilen UV radyasyonu neticesi ortaya çıkan DNA foto ürünleri (pirimidin yıpranma çiftleri) gibi (11).
Deri aynı zamanda sigara içimi, araba egzoz gazı ve endüstri artıkları gibi başka DNA harabiyetine yol açan maddelere de maruz kalır. Sigara dumanı hücrelerin kimyasal benzoprene maruz kalmasına yol açar ki bu madde DNA'daki guanin bazlarıyla birleşerek değişik yapılar oluşturur (12). Böylece yaşlanma hem genetik bir programın hem de sürekli bir yıpranma prosesinin hücresel DNA proteinlerini tahrip etmesine, böylece hücresel fonksiyonun yaşlanması ve ölümüne neden olur.
Deri yaşlanması iki olgunun sonucudur. 1- İntrensek (kronolojik) yaşlanma: Bu tip yaşlanma sadece zamana bağlı olarak oluşan değişiklikleri içerir. 2- Foto-Yaşlanma ise, çevresel etkilere, özellikle de güneş harabiyetine bağlı olarak gelişen yaşlanma sürecidir (13).
İntrensek yaşlanma özellikle derinin fonksiyonlarında fizyolojik değişikliklerle karakterize, kaçınılmaz, evrensel bir olaydır. Bunun aksine foto-yaşlanma ise, ne evrensel ne de kaçınılmazdır. Foto yaşlanma güneşe maruz kalan deride oluşan morfolojik ve fizyolojik değişikliklerle karakterizedir (13).
YAŞLI DERİNİN İNTRENSEK ÖZELLİKLERİ
Klinik olarak zamana bağlı kronolojik yaşlı deri kuru ve soluk görünür. İnce kırışıklıklar mevcuttur. Laksisite bir ölçüde artmış ve bir dizi iyi huylu neoplazm (tümör) oluşmuştur. Histolojik olarak bu tip yaşlanmada en önemli ve çarpıcı değişiklik ise dermo-epidermal bileşkenin düzleşmesidir. Bunun sonucu olarak dermis ve epidermis arasındaki yüzey küçülmüştür. Öyle ki, bu küçülmeden dolayı derinin her iki tabakası arası iletişim ve besin maddelerinin transferi azalmıştır (14).
Stratum korneumun intrensek yaşlanmada ortalama kalınlığı pek değişmemektedir. Ancak, st.korneumun bariyer işlevini sağlayan nötral lipitlerin oluşum hızı azalmaktadır (15). Ayrıca, çoğunluğu kıl foliküllerinde daha fazla olmak üzere melanosit yoğunluğu da sürekli bir düşüş göstermektedir. 50 yaş ve üzerindeki nüfusun saçlarında pigment azlığına bağlı olarak beyazlaşma (kırlaşma) da görülmektedir(16). Son zamanlarda anagen faz sırasında melanositik kök hücrelerinin gelişme ve/veya göçleri kök hücre sinyal faktörlerine kuvvetle bağımlı oldukları ileri sürülmüştür (17, 18). Diğer sitokinler de olduğu gibi yaşlanmayla kök hücre faktörlerinin üretiminin azalacağı muhtemeldir. Böylece yeni oluşacak kıl foliküllerinde yoğunlaşacak ve ulaşacak melanosit yeteneği sınırlanmış olmaktadır. Yaşa bağlı olan diğer epidermal değişiklikler ise epidermal langerhans hücrelerinin sayısında bariz bir azalmayı da içerir. Bilindiği gibi antigen sunan bu hücrelerin bağışıklık sisteminde de önemli rolü vardır. Geri kalan diğer hücrelerin dendritik uzantılarında kısalmayı içeren bir dizi morfolojik anormallikler oluşur (19). Ara maddenin ve kollajenin üretimlerinin azalması ve parçalanmanın (degradasyon) artması sonucu olarak miktarlarının azalması dermiste hacim kaybına neden olur (20). Özellikle elastik liflerin çok fazla parçalandığını gözleriz. Ayrıca, yaşlanmayla damar duvarı kalınlığında farklılıklar oluşabilir. Bazı damarlarda kalınlaşmalar, bazılarında ise neredeyse yarısına varan incelmeler gözlenir. Bazı damar duvarlarında ise damar çevresi hücrelerinde azalma veya tamama yakın yok olma söz konusudur. Üstelik dermal papillaları dolduran kılcal damarların damar yatakları da kaybolmuştur (20). Damarsal ağdaki yaşa bağlı bu değişiklikler ekrin ve apokrin bezlerin yaşa bağlı atrofisinde rol oynarlar. Bu paragraftaki değişiklikler figür 1'de gösterilmiştir.
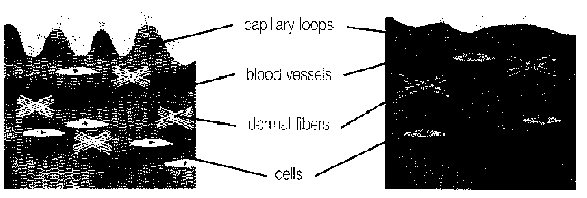
İntrensek yaşlanma neticesi gelişen işlevsel fonksiyonel değişiklikler yara iyileşmesinin de yavaş olmasına neden olur. Çünkü keratinosit ve fibroblastların çoğalma kapasitesi azalmıştır, sitokin üretimi yavaşlamıştır, kollajen ve elastik lif sentezi düşmüştür, keratinositlerin terminal (st.korneum) farklılaşma yetenekleri azalmıştır (21). Bu arada gençlere nispeten yaşlılarda derinin bariyer fonksiyonu da kolayca bozulabilir ve yaşlılarda st.korneumun oluşumu için gereken zaman ikiye katlanmıştır (15). İlginç olarak kadın hormonlarının belirgin derecede st.korneumun sphingolipid kompozisyonunu etkilediği rapor edilmiştir. Bu da yaşlılarda hormonların azalmasının bariyer fonksiyonunu değiştirebileceğini göstermektedir. Kadınlarda ayrıca menopoz sonrası yıllarda kemik ağırlığı ve deri kollageni de hızla düşer, bu da bize hormonların kollagen sentezi ve parçalanması üzerinde etkili olduğunu düşündürür.
Yaşlanmayla beraber keratinosit sitokinlerinin azalması bağışıklık sisteminin duyarlılığını da azaltır. Melanosit sayılarının azalması da vücudun ultraviyole ışınlarına karşı koruyucu bariyerinin azalmasına neden olur ve yaşlılarda UV'ye bağlı DNA harabiyetinin oluşumuna daha eğilimli kılar. Üstelik yaşlılarda DNA onarım oranı da azalmıştır ve böylece deri kanserlerinin gelişim riski artmıştır (24). İlginç olarak son bir çalışmada DNA harabiyetinin onarımına katılan proteinlerin seviyesinde de yaşa bağlı düşüşler görülmüştür (25). Özel olarak çekirdek onarım prosesine katılan proteinlerin seviyesi yaşlı kişilerden alınan firoblastlarda, gençlere nazaran daha düşüktür. Bu bulgu yaşlanmayla kanser sıklığında artış arasındaki bağlantıyı açıklamaktadır (26).
Yaşlanmayla insan epidermisinde azalan bir önemli endokrinolojik fonksiyon da D vitamininin üretimidir. Normalde güneş ışınları epidermisdeki D vitamininin prekürsörlerini aktifleyerek daha sonra D3 (7 dehidro kolesterol) vitaminine dönüşecek olan previtamin D3'e dönüştürülür. Yaşlanmayla epidermisteki prekürsör vitamin D3 miktarı düşer, bu da yaşlılarda D3 vitamininin azalmasına neden olur (27, 28). Nihayet damar yatağındaki değişiklikler yaşlılarda sık görülen damarsal kırılmalara neden olur. Ayrıca, dermal damar yatakları ve damar duvarlarının yapısı vücudun ısısını ayarladığından bu durum yaşlılarda sıcak ve soğuktan aşırı etkilenmeye neden olur (20). Yaşlılıkta azalan insan derisi fonksiyonları aşağıda özetlenmiştir.
YAŞLILIKLA İNSAN DERİSİNDE AZALAN FONKSİYONLAR
- Hücre yenilenmesi,
- Bariyer fonksiyonu,
- Kimyasal arınma,
- Hislerin algılanmasında azalma,
- Mekanik korunmada,
- Yara iyeleşmesinde,
- İmmün cevaplarda,
- Isı ayarlanmasında,
- Ter salgılanmasında,
- Yağ salgılanmasında,
- D vitamini üretiminde,
- DNA onarımında azalma.
FOTO YAŞLANMANIN KARAKTERİSTİK ÖZELLİKLERİ
Klinik olarak güneşe bağlı harabiyette deri kuru, soluk, ince ve derin kırışıklıklar şeklinde görülür (20). Yüzde bazen siyah komedonlarla karakterize kabarcıklar görülebilir (Favre - Racouchot hastalığı). Diğer değişiklikler arasında çok sayıda damar çatlaması (Telenjiektazi) ve çiller, güneş lekeleri ve damlacık şeklinde beyaz lekelerle karakterize düzensiz pigmentasyon bozuklukları vardır. Aynı zamanda foto-yaşlanmada aktinik keratoz gibi bir dizi prekanseröz döküntü de vardır (20).
Epidermis güneşe karşı korunmuş kişilerle mukayese edildiğinde ileri derecede atrofik veya tersine hiperplastik görünümdedir. Keratinositler sıklıkla atipik organizasyonlar gösterirler (29). Melanositler bazal tabakada yer yer artmış veya azalmış dizilimler gösterirler (20). Langerhans hücrelerinin sayısında da bariz bir azalma dikkati çeker.
Ancak foto-yaşlanmada temel mikroskobik değişiklik elastolizisdir. Bunun anlamı papiller dermisin içerisinde anormal amorf elastik bir maddenin mevcudiyetidir. Elastik lifler parçalanmış bir görünümdedirler.
Kronik yaşlanmada dermis hücrelerinde azalma gözlenirken foto yaşlanmada sıklıkla mast hücreleri, histiyositler, mononükleer hücreler ve fibroblastlarda artma gözlenir. Hatta dermisin içinde lenfosit birikimine de heliodermatit (güneş dermatiti) denilir (30).
Kollagen ve elastik liflerde dejeneratif değişiklikler gözlenir (metalloproteaz ve sitokin aktivitesinde artma (29), ve matriks protein sentezindeki azalmaya bağlı olarak). Aynı zamanda epidermisin hemen altındaki küçük damarlarda güneşten korunan kişilerde azalma gözlenirken foto-yaşlanma durumunda, derideki kan damarları genişlemiş, düzensizleşmiş ve bazal membranları kalınlaşmış görülür (30).
Foto-yaşlanmada da yara iyileşmesi ve immün cevaplarda azalma görülür.
SİGARA İÇENLERİN DERİ ÖZELLİKLERİ
Özellikle bayanlarda sigara iç ve dış yaşlanmayı tetikler (31, 32). Sigara içen bireylerde kırışıklığın yanı sıra derinin grimsi bir renk aldığı gözlenir. Çalışmalar yukarıdaki deri bulgularının şiddetinin, artan sigara sayısıyla direkt bağlantılı olduğunu göstermiştir.
Mikroskobik olarak sigara içenlerin dermisinde elastik lifler parçalanmış ve kalınlaşmıştır. Elastik liflerdeki bu değişikliğin yapısı foto-yaşlanmadakine benzerlik gösterir. Ancak, sigara içenlerin derisindeki elastik lif değişiklikleri sadece papiller dermiste değil (foto-yaşlanmadaki gibi) retüküler dermiste de mevcuttur (33).
Sigara içmenin ROS oluşumunu artırarak kronik dermal iskemiye neden olan (dermisin kanlanamaması) prooksidan etkisi de bilinir. Ayrıca, derinin ROS'u kontrol etme kapasitesi sigara içenlerde azalmıştır. Çünkü, sigara derideki A vitamini seviyesini azaltır. Bu da derinin serbest kalan aşırı oksijene karşı işlevini yavaşlatmakta ve UV ışınlarına karşı korumasız bırakmaktadır. Ayrıca, sigara içenlerin derisinde bulunan nötrofiller elastaz aktivitesini artırarak sigara içenlerin derisinde östrojen seviyesini azaltır. Bu da östradiol hidroksilasyonunu hızlandırır (32).
İlginç olarak sigara içen bireylerde içmeyenlere nazaran deri kanseri prevalansı artmıştır. Muhtemelen bu durum, deri hücrelerinin DNA harabiyetine yol açan benzopirenin sigara dumanındaki mevcudiyetinden kaynaklanır. Bu madde önemli bir mitojendir ve kötü tabiatlı dönüşümlere imkan verir.
GEN VE PROTEİN EXPRESYONUNDA YAŞA BAĞLI DEĞİŞİKLİKLER
Hücre yenilenmesi yaşlılıkta azaldığından bazı araştırmacılar hücre yenilenme evrelerine katılan genlerin expresyonundaki değişiklikleri incelemişlerdir (34). Bu çalışmaların neticesinde hücre yenilenme sürecinde gerekli olan mekanizmaların ve düzenli gen diziliminin yaşlılıktaki hücre faaliyetleri esnasında bozulduğunu düşündürecek niteliktedir.
KAYNAKÇA
1- Balin AK, Allen RG: Molecular Bases of Biologic Aging. In BA Gilchrest (ed.) Clinics in Geriatric Medicine. Philadelphia, WB Saunders, 1989, p.1.
2- Blackburn EH: Sutructure and function of telomeres. Nature 350: 569, 1991.
3- Allsopp RC: Telomere length predicts replicative capacity of human fibroblasts. Proc Natl Acad Sci USA. 89: 10114, 1992.
4- Vaziri H and Benchimol S: From telomere loss to p53 induction and activation of a DNA - damage pathway at senescence: the telomere loss/DNA damage model of cell aging. Exp Gerontol 31: 295, 1996.
5- Beauregard S, Gilchrest BA. Syndromes of premature aging. Dermatol Clin. 5: 109, 1987.
6- Yu Ce, Oshima J, Fu YH, et al. Mulligan J and Schellenberg GD: Positional cloning of the Werner's syndrome gene. Science. 272: 258, 1996.
7- Troelstra C, van Gool A, de Wit J, Vermeulen W, Bootsma D: ERCC6, a member of a subfamily of putative helicases, is involved in Cockayne's syndrome and preferential repair of active genes. Cell. 7: 939, 1992.
8- Savitsky K,: A single ataxia telangiectasia gene with a product similar to PI-3 kinase. Science. 268: 1749, 1995.
9- Johnson TE: Aging can be genetically disected into component processes using long-livid lines of Caenorhabditis elegans. Proc Natl Acad Sci USA. 84: 3777, 1987.
10- Sun J, Kae SP, Childress AM, Pinswasdi C, Jazwinski SM: Divergent roles of RAS1 and RAS2 in yeast longevity. J Biol Chem. 269: 18638, 1994.
11- Kripke M.: Carcinogenesis: Ultraviolet Radiation. In Dermatology in General Medicine. New York, McGraw-Hill, 1999, p. 465.
12- Phillips DH: Fifty years of benzo(a)pyrene. Nature 303: 468, 1983.
13- Balin AK, Kligman AM: Aging and the skin. New York, Raven 1989.
14- Fenske NA and Lober CW: Structural and functional changes of normal aging skin. J Am Acad Dermatol, 15: 571, 1986.
15- Ghadially R, Brown BE, Sequeira-Martin SM et al. The aged epidermal permeability barrier. Structural, functional, and lipid biochemical abnormalities in humans and a senescent murine model. J Clin İnvest. 95: 2281-2290, 1995.
16- Keogh EV, Walsh RJ. Rate of greying uf human hair. Nature. 207: 877-878, 1965.
17- Botchkareva NV, Khlgatian M, Longley BJ et al. SCF/c-kit signaling is required for cyclic regeneration of the hair pigmentation unit. FASEB J. 15: 645-658, 2001.
18- Tobin DJ, and Paus R. Graying: gerontobiology of the hair follicle pigmentary unit. Exp Gerentol. 36: 29-54, 2001.
19- Sauder DN: Effect of age on epiudermal immune function. Dermatol Clin 4: 447, 1986.
20- Yaar M, and Gilchrest BA: Aging of Skin. In IM Freedberg, AZ Eisen, K Wolff, KF Austen, LA Goldsmith, Sl Katz, TB Fitzpatrick (eds.) Dermatology in General Medicine, New York, McGraw-Hill, p 1697, 1999.
21- Gerstein Ad, Phillips TJ, Rogers GS, Gilchrest BA: Wound healing and aging. Dermatol Clin 11: 749, 1993.
22- Denda M, Koyama J, Hori J et al. Age-and sex-dependent changes in stratum corneum sphingolipids. Arch Dermatol Res. 285: 415-417, 1993.
23- Castelo-Branco C, Pons F, Gratacos E, et al. Relationship between skin collagen and bone changes during aging. Maturitas 18: 199, 1994.
24- Hadshiew I, Eller M, Gilchrest BA: Age-Associated Decrease in Human DNA Repair Capacity: Implications for the Skin. Age 22: 45, 1999.
25- Goukassian D, Gad F, Yaar M, et al. Mechanism and implications of the age-associateddecrease in DNA repair capacity. FASEB J 14: 1325-1334, 2000.
26- Kricker A, Armstrong BK, and Parkin DM: Measurement of skin cancer incidence. Health Rep 5: 63, 1993.
27- Holick MF, McLaughlin JA, Parrish JA, Anderson RR: The photochemistry and photobiology of vitamen D3. In JD Regan, JA Parrish, (eds.) The Science of Photomedicine New York, Plenum 1983, p195.
28- Holick MF, Matsuoka LY, and Wortsman J: Age, vitamin D, and solar ultraviolet. Lancet 2: 1104, 1989.
29- Bhawan J, Andersen W, Lee J, Labadie R, Solares G: Photoaging versus intrinsic aging: a morphologic assessment of facial skin. J Cutan Pathol 22: 154, 1995.
30- Kligman AM and Kligman LH: Photoaging. In: IM Freedberg, Az Eisen, K Wolff, KF Austen, LA Goldsmith, SL Katz, TB Fitzpatrick (eds.) Dermatology in General Medicine. New York, McGraw-Hill, p 1717.
31- Davis BE and Koh HK: Faces going up in smoke. A dermatologic opportunity for cancer prevention. Arch Dermatol 128: 1106, 1992.
32- Smith JB and Fenske NA: Cutaneous manifestations and consequences of skoking. J Am Acad Dermatol 34: 717, 1996.
33- Frances C, Boisnic S, Hartmann DJ, et al: Changes in the elastic tissue of the non-sun-exposed skin of cigarette smokers. Br J Dermatol 125: 43, 1991.
34- Yaar M and Gilchrest BA: Aging versus photoaging: Postulated mechanism and effectors. J Invest Dermatol Symp Proc 3: 47-51, 1998.
*Professor of Dermatology, Boston University, USA
**Gazi Üniversitesi Mesleki Eğitim Fakültesi Güzellik Bilgisi
ABD
Beşevler/ ANKARA
|

